BYDUREON® exénatide
Bydureon® (suspension injectable d'exénatide à libération prolongée en stylo pré-rempli) est un agoniste du récepteur du glucagon-like peptide-1 (GLP-1), injectable une fois par semaine, présenté sous forme d'un stylo unidose, indiqué pour améliorer le contrôle glycémique chez les adultes atteints d'un diabète de type 2.
À propos de Bydureon
¶¶Le risque d'hypoglycémie est augmenté lorsque Bydureon stylo est utilisé en association à un sulfamide hypoglycémiant ou avec d'autres sécrétagogues glucose-indépendants (par ex., méglitinides). Les cliniciens pourront considérer une réduction de la dose de sulfamide hypoglycémiant.
***Bydureon n'est pas indiqué pour la prise en charge de la perte de poids, et la modification du poids était un critère d'évaluation secondaire dans des essais cliniques.
†††Bydureon n'est pas indiqué pour la prise en charge des facteurs de risque liés à la MCV, qui étaient des critères d'évaluation secondaires dans des essais cliniques.
Pharmacologie
Pharmacocinétique de Bydureon
Revue de l'inclusion d'exénatide dans une technologie des microsphères
Titre : Encapsulation of exenatide in poly-(D,L-lactide-co-glycolide) microspheres produced an investigational long-acting once-weekly formulation for Type 2 diabetes
Auteurs : DeYoung MB, MacConell L, Sarin V, et al.
Référence : Diabetes Technol Ther 2011;13:1145–54
Consulter le résumé de cet article de Young MB, et al. publié dans Diabetes Tech Ther
Pharmacocinétique, efficacité et sécurité de Bydureon : Étude de preuve de concept
Titre : Effects of once-weekly dosing of a long-acting release formulation of exenatide on glucose control and body weight in subjects with type 2 diabetes
Auteurs : Kim D, MacConell L, Zhuang D, et al.
Référence : Diabetes Care 2007;30:1487–93
Consulter le résumé de cet article de Kim D, et al. publié dans Diabetes Care
Mécanisme d'action
Bydureon : Le seul AR GLP-1 qui utilise la technologie des microsphères pour une administration une fois par semaine3, 19
La technologie des microsphères biodégradables de Bydureon permet :
- une exposition systémique, continue à l'exénatide grâce à une administration hebdomadaire3, 19
- Régulation dynamique des taux de glycémie avec des concentrations maximales-minimales moindres pour une tolérance améliorée par rapport à des injections quotidiennes 3, 5, 12, 14
- Aucun besoin de titration et possibilité de modifier le jour de l'administration si nécessaire7
Un système de délivrance unique qui permet une présence constante d'exénatide12, 19
BYDUREON une fois par semaine est conçu pour délivrer des niveaux thérapeutiques uniformes d'exénatide au fil du temps12
L'encapsulation en microsphères permet une libération continue d'exénatide au fil du temps12
Adapté avec la permission de DeYoung, et al.12
Bydureon agit de façon glucose-dépendante
Activités hypoglycémiantes de Bydureon
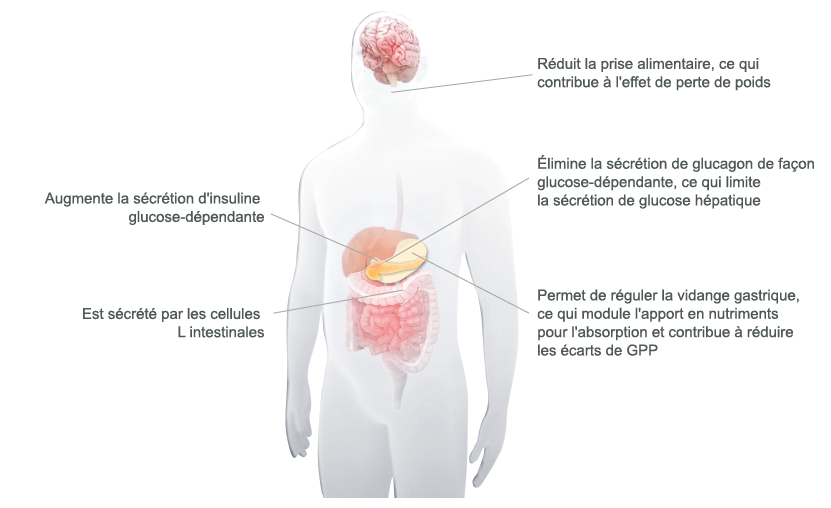
Le GLP-1 agit en plusieurs endroits de l'organisme3, 20-22 :
- Le GLP-1 est une hormone incrétine importante, qui joue un rôle dans l'homéostasie du glucose3, 20, 22
Bénéfices pour les patients
Traitement avec une longue expérience
Avec plus de 4,1 millions d'années-patient environ23
Avec plus de 4,1 millions d'années-patient24
Abréviation : AR GPL-1, agoniste du récepteur du glucagon-like peptide-1
Données cliniques et études en cours
- 170 études achevées avec des résultats pour l'exénatide25
- 73 études en cours25
- > 13 000 patients inclus dans les études en cours23
- 2 242 publications différentes26
- Données sur 7 ans27, 28
- Plus de 12 ans d'expérience clinique avec l'exénatide
Pratique
- Première molécule de la classe des GLP1-RA au niveau mondial
- Premier traitement contre le diabète de type 2 administré une fois par semaine
- Plus de 10 ans d'expérience en pratique clinique
Le stylo Bydureon est conçu pour délivrer des doses thérapeutiques constantes d'exénatide au cours du temps12
Le stylo Bydureon fournit des doses thérapeutiques constantes, jour après jour, semaine après semaine5,19
Du fait de variances dans les dosages, les schémas posologiques et la conception de l’étude, aucune comparaison directe avec les autres AR GLP-1 ne peut être réalisée
Abréviation : ES, erreur standard
Bydureon en stylo est le seul AR GLP-1 encapsulé dans des microsphères, qui permet une libération prolongée et uniforme.3, 5
Conception de l’étude
Le profil pharmacocinétique de BYDUREON a été déterminé dans un essai de 30 semaines, randomisé, en ouvert, avec comparateur actif. Les concentrations plasmatiques d'exénatide ont été mesurées chez 129 patients recevant BYDUREON.5, 19
L'observance était significativement meilleure que celle avec les AR GLP-1 quotidiens29
Observance du traitement par des AR GLP-129
Risque relatif avec IC à 95 % (faible = mauvaise observance par rapport à l'exénatide 1x/sem)
‡‡‡P < 0,001 pour l'exénatide 1x/sem par rapport aux agents comparateurs.
Odds ratio de l'observance ajusté par une régression logistique à variables multiples (parvenant à une proportion de jours couverts de 90 %) au cours de la période de suivi de 6 mois, avec l'exénatide 1x/sem comme référence (n = 22 838).29
66 % des patients recevant le BYDUREON en stylo sont restés sous traitement pendant 3 ans (156 semaines) et 59 % pendant 5 ans.6, 8
- Un traitement une fois par semaine par le stylo BYDUREON peut encore améliorer l'observance du traitement29
Conception de l’étude
Patients naïfs d'AR GLP-1 atteints d'un diabète de type 2 ayant commencé un AR GLP-1 (exénatide 2x/j, exénatide 1x/sem ou liraglutide 1x/j) ont été suivis pendant 6 mois pour mesurer et comparer leur observance à l'AR GLP-1 qu'ils avaient commencé.29
Abréviations : 2x/j, deux fois par jour ; AR GLP-1, agoniste du récepteur du glucagon-like peptide-1 ; 1x/j une fois par jour ; 1x/sem, une fois par semaine
Étude CGM : Bydureon a permis de réduire le taux moyen de glucose pendant toute la journée4
Glycémie moyenne sur 24 heures à la référence, et aux semaines 4 et 104
Les courbes représentent une moyenne de tous les patients de l'étude. Ceci n'est pas une représentation des épreuves pré ou post-prandiales
§§§La fourchette euglycémique dans cette étude inclut à la fois la GAJ et la GPP.
Réduction significative de la glycémie moyenne pondérée sur 24 heures à 4 semaines et 10 semaines.4
Réduction de la glycémie moyenne pondérée sur 24 heures ajustée au placebo4:
- À la semaine 4 : -17,8 mg/dl
- À la semaine 10 : -30,2 mg/dl
Conception de l’étude
Données démographiques des patients à la référence (mITT) : BYDUREON + MXR : 55 % d'hommes ; 86,7 % de caucasiens ; durée moyenne du diabète de type 2, 9,01 ans ; HbA1c moyen, 8,17 % ; GAJ moyenne, 178 mg/dl ; GPP moyenne pondérée sur 2 heures 221,6 mg/dl. Placebo + MXR : 57 % d'hommes ; 82 % de Caucasiens ; durée moyenne du diabète de type 2, 9,92 ans ; HbA1c moyen, 7,98 % ; GAJ moyenne, 167,( mg/dl ; GPP moyenne pondérée sur 2 heures, 221,6 mg/dl.4
Une étude randomisée en double aveugle comparant BYDUREON versus placebo chez 116 patients atteints de diabète de type 2, âgés de ≥ 18 ans et ≤ 75 ans, traités par une dose stable de MXR (≥ 1 500 mg/jour depuis au moins 8 semaines) avec un contrôle inadéquat de la glycémie (HbA1c ≥ 7 % et ≤ 10 %). Après les 4 semaines d’initiation durant laquelle les patients étaient traités par MXR en ouvert, les patients ont été randomisés en 1:1 pour recevoir BYDUREON (2 mg) + MXR ou le placebo + MXR. Un système de SCG a été utilisé pour mesurer la glycémie 24 heures sur 24 durant la phase d'initiation (Jour -8 et Jour –1), à la semaine 4 (jours 21 à 28) puis à la semaine 10 (jours 63 à 70) du traitement. L’étude se terminait avec un suivi de sécurité de 4 semaines. Le critère d’évaluation principal était la modification du glucose moyen pondéré sur 24 heures par rapport à la référence après 4 et 10 semaines de traitement. Les critères d’évaluation secondaires évalués aux semaines 4 et 10 du traitement incluaient : GAJ, GPP sur 2 heures et la proportion de temps passé par les patients en fourchette hyperglycémique (> 180 mg/dl), hypoglycémique (< 70 mg/dl) ou euglycémique (≥ 70 à ≤ 180 mg/dl – la fourchette inclut les périodes à jeun et post-prandiales).4
Bydureon a augmenté le temps passé dans la fourchette euglycémique par comparaison avec la référence4
Proportion (%) du temps passé dans la fourchette euglycémique (≥ 70 à ≤ 180 mg/dl) à la référence, à 4 semaines et 10 semaines4
- Dès 4 semaines, ainsi qu'à 10 semaines, BYDUREON a réduit l'exposition des patients à des niveaux de glucose sanguin en dehors de la fourchette euglycémique (> 180 mg/dl et < 70 mg/dl) par rapport à la référence tout au long de la période de 24 heures4
- BYDUREON a démontré une amélioration constante par rapport à la référence, les patients passant 77 % de leur journée dans la fourchette euglycémiqueǁǁǁ à 10 semaines4
- Le temps passé dans la fourchette hypoglycémique n’a pas augmenté significativement à 4 et 10 semaines4
ǁǁǁLa fourchette euglycémique dans cette étude inclut à la fois la GAJ et la GPP.
Conception de l’étude
Données démographiques des patients à la référence (mITT) : BYDUREON + MXR : 55 % d'hommes ; 86,7 % de caucasiens ; durée moyenne du diabète de type 2, 9,01 ans ; HbA1c moyen, 8,17 % ; GAJ moyenne, 178 mg/dl ; GPP moyenne pondérée sur 2 heures 221,6 mg/dl Placebo + MXR : 57 % d'hommes ; 82 % de Caucasiens ; durée moyenne du diabète de type 2, 9,92 ans ; HbA1c moyen, 7,98 % ; GAJ moyenne, 167,5 mg/dl ; GPP moyenne pondérée sur 2 heures, 221,6 mg/dl.4
Une étude randomisée en double aveugle comparant BYDUREON versus placebo chez 116 patients atteints de diabète de type 2, âgés de ≥ 18 ans et ≤ 75 ans, traités par une dose stable de MXR (≥ 1 500 mg/jour depuis au moins 8 semaines) avec un contrôle inadéquat de la glycémie (HbA1c ≥ 7 % et ≤ 10 %). Après les 4 semaines d’initiation durant laquelle les patients étaient traités par MXR en ouvert, les patients ont été randomisés en 1:1 pour recevoir BYDUREON (2 mg) + MXR ou le placebo + MXR. Un système de SCG a été utilisé pour mesurer la glycémie 24 heures sur 24 durant la phase d’initiation (Jour -8 et Jour –1), à la semaine 4 (jours 21 à 28) puis à la semaine 10 (jours 63 à 70) du traitement. L’étude se terminait avec un suivi de sécurité de 4 semaines. Le critère d’évaluation principal était la modification du glucose moyen pondéré sur 24 heures par rapport à la référence après 4 et 10 semaines de traitement. Les critères d’évaluation secondaires évalués aux semaines 4 et 10 du traitement incluaient : GAJ, GPP sur 2 heures et la proportion de temps passé par les patients en fourchette hyperglycémique (> 180 mg/dl), hypoglycémique (< 70 mg/dl) ou euglycémique (≥ 70 à ≤ 180 mg/dl – la fourchette inclut les périodes à jeun et post-prandiales).4
Bydureon a amélioré la GPP et la GAJ par rapport à la référence, à 4 et 10 semaines4
GPP à 2 heures : Réduction significative à 4 et à 10 semaines4
GAJ : Réduction significative à 4 et à 10 semaines4
Les données sont les moyennes +/- ES au jour 2 de chaque semaine
Analyse de mesures répétées.
Étude SCG : BYDUREON a systématiquement réduit la GAJ.4
Conception de l’étude
Données démographiques des patients à la référence (mITT) : BYDUREON + MXR : 55 % d'hommes ; 86,7 % de caucasiens ; durée moyenne du diabète de type 2, 9,01 ans ; HbA1c moyen, 8,17 % ; GAJ moyenne, 178 mg/dl ; GPP moyenne pondérée sur 2 heures 221,6 mg/dl. Placebo + MXR : 57 % d'hommes ; 82 % de Caucasiens ; durée moyenne du diabète de type 2, 9,92 ans ; HbA1c moyen, 7,98 % ; GAJ moyenne, 167,5 mg/dl ; GPP moyenne pondérée sur 2 heures, 221,6 mg/dl.4
Une étude randomisée en double aveugle comparant BYDUREON versus placebo chez 116 patients atteints de diabète de type 2, âgés de ≥ 18 ans et ≤ 75 ans, traités par une dose stable de MXR (≥ 1 500 mg/jour depuis au moins 8 semaines) avec un contrôle inadéquat de la glycémie (HbA1c ≥ 7 % et ≤ 10 %). Après les 4 semaines d’initiation durant laquelle les patients étaient traités par MXR en ouvert, les patients ont été randomisés en 1:1 pour recevoir BYDUREON (2 mg) + MXR ou le placebo + MXR. Un système de SCG a été utilisé pour mesurer la glycémie 24 heures sur 24 durant la phase d’initiation (Jour -8 et Jour –1), à la semaine 4 (jours 21 à 28) puis à la semaine 10 (jours 63 à 70) du traitement. L’étude se terminait avec un suivi de sécurité de 4 semaines. Le critère d’évaluation principal était la modification du glucose moyen pondéré sur 24 heures par rapport à la référence après 4 et 10 semaines de traitement. Les critères d’évaluation secondaires évalués aux semaines 4 et 10 du traitement incluaient : GAJ, GPP sur 2 heures et la proportion de temps passés par les patients en fourchette hyperglycémique (> 180 mg/dl), hypoglycémique (< 70 mg/dl) ou euglycémique (≥ 70 à ≤ 180 mg/dl – la fourchette inclut les périodes à jeun et post-prandiales).4
Autres
Développement et maniabilité du dispositif d'injection de Bydureon
Étude de maniabilité du dispositif d'injection unidose de Bydureon
Titre : Application of adult-learning principles to patient instructions: A usability study for an exenatide once-weekly injection device
Auteurs : Lorenzi G, Schreiner B, Osther J, Boardman M
Référence : Clin Diabetes 2010;28:157–62
Consultez cet article de Lorenzi G, et al. publié dans Clin Diabetes
Besoin non satisfait
La GPP et la GAJ contribuent à l'HbA1c30
La GPP contribue davantage à l'hyperglycémie globale que la GAJ à de faibles taux d'HbA1c¶¶¶30
Adapté avec la permission de Monnier et al.
Les écarts de GPP sont un facteur majeur contribuant à la charge glycémique globale chez les patients présentant une hyperglycémie légère à modérée.30
Conception de l’étude
Étude observationnelle (N = 290) chez des patients traités depuis au moins 3 mois par régime alimentaire seul, metformine, glyburide, ou les deux. Les critères d’inclusion étaient un antécédent de diabète de type 2 depuis ≥ 6 mois et aucun traitement en cours par insuline ou acarbose. Les patients ont été triés en fonction de leur taux moyen d'HbA1c (%), et une analyse sur 1 jour, à 4 points, des concentrations plasmatiques en glucose, à jeun et post-prandiale, a été réalisée après l'administration d'un régime alimentaire normalisé.30, 31
¶¶¶Les patients ont été traités par régime alimentaire seul, par metformine, par glyburide, ou par une association de metformine et de glyburide.
L'insuline basale peut ne pas contrôler de façon adéquate les élévations de GPP32
Contributions relatives de la GPP et de la GAJ à l'hyperglycémie après 24 ou 28 semaines de traitement par insuline basale32
Adapté avec la permission de Riddle, et al.
La GPP peut rester élevée et contribuer à l'hyperglycémie globale même chez les patients traités par insuline basale32
De nombreux patients ne parviennent néanmoins pas à atteindre leurs objectifs en termes d'HbA1c après le traitement par insuline basale.33, 34
Conception de l’étude
Des données de référence et à 24 semainesa issues de 6 études menées chez des patients (N = 1 699) atteints de diabète sucré de type 2 mal contrôlé (HbA1c > 7 %) sous antihyperglycémiques oraux ont été agrégées pour analyse. Le taux d'HbA1c moyen à la référence était de 8,7 % pour la population de patients avant l'augmentation posologique du traitement par insuline basale (n = 1 261). Les concentrations plasmatiques de glucose à jeun et de GPP ont été dérivées de mesures relevées avant et 2 heures après chaque repas et au coucher.32
aLes données des patients issues d'une étude n'ont pas été évaluées à 24 semaines. Celles-ci ont été substituées par les données à 28 semaines.32