Cancer du sein
Mécanisme d’action
L’olaparib est un puissant inhibiteur des enzymes poly (ADP-ribose) polymérase humaines (PARP-1, PARP-2 et PARP-3) et il a été montré qu'il inhibait la croissance de certaines lignées de cellules tumorales in vitro et la croissance tumorale in vivo soit en monothérapie soit en association avec des chimiothérapies de référence.1
Les tumeurs BRCAm ont une biologie moléculaire unique qui les rend sensibles à l'inhibition de la PARP.3,4
Lynparza inhibe la PARP de deux façons:*3-5
- En inhibant l’activité enzymatique3-5
- En augmentant la formation de complexes PARP-ADN piégés3-5
In vitro activity does not always correlate with clinical efficacy.
*The exact mechanism of action of LYNPARZA remains a subject of research.
PARP=poly (ADP-ribose) polymerase; PARPi=poly (ADP-ribose) polymerase inhibitor
Résumé des résultats
Cancer du sein précoce (étude OlympiA)
Conception de l’étude OlympiA
L’étude OlympiA étudiait la sécurité d’emploi et l’efficacité de l’olaparib en traitement adjuvant chez des patients atteints d’un cancer du sein précoce à haut risque HER2-négatif et présentant une mutation germinale des gènes BRCA1/2 qui ont terminé un traitement local définitif et une chimiothérapie néoadjuvante ou adjuvante.1
BID=twice daily; CPS + EG=Clinical stage, oestrogen receptor status, grade, and post-treatment pathologic stage scoring system; DDFS=distant disease-free survival; eBC=early breast cancer; gBRCAm=germline BRCA-mutated; HER2=human epidermal growth factor receptor-2; HR+=hormone receptor-positive; HRQoL=health-related quality of life; IDFS=invasive disease-free survival; OS=overall survival; pCR=pathological complete response; pN=positive lymph node; pT=primary tumour pathological size; TNBC=triple-negative breast cancer.
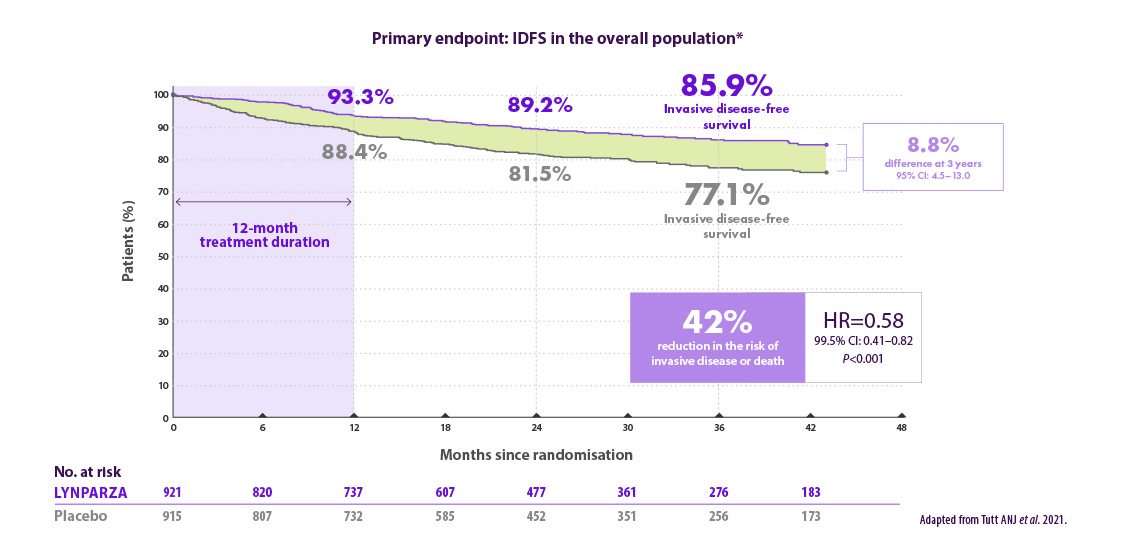
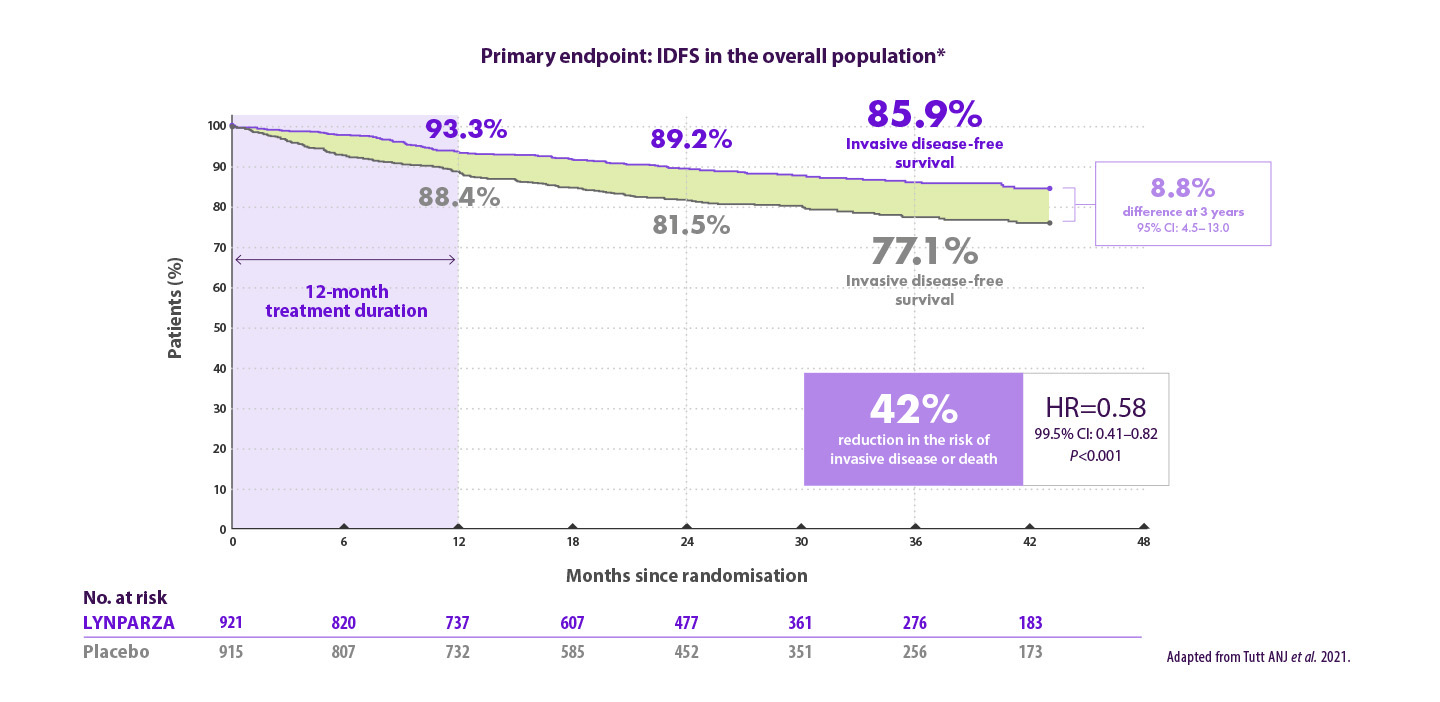
Résultats d’efficacité pour le traitement adjuvant des patients atteints d’un cancer du sein précoce avec mutation germinale des gènes BRCA dans l’étude OlympiA
Lynparza® réduit de 42% le risque de maladie invasive par rapport au placebo6
*Based on a pre-specified event driven interim analysis with a median follow-up of 2.5 years. CI=confidence interval; HR=hazard ratio; IDFS=invasive disease-free survival.
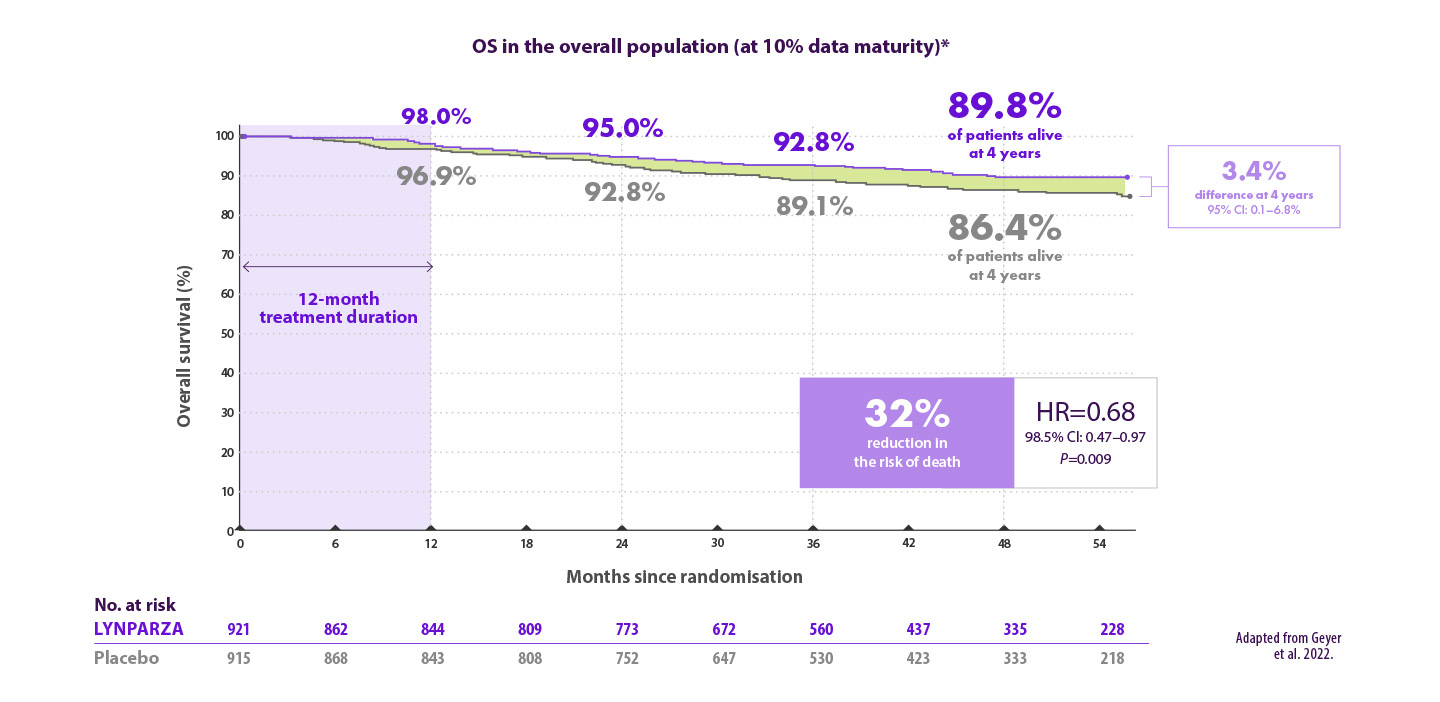
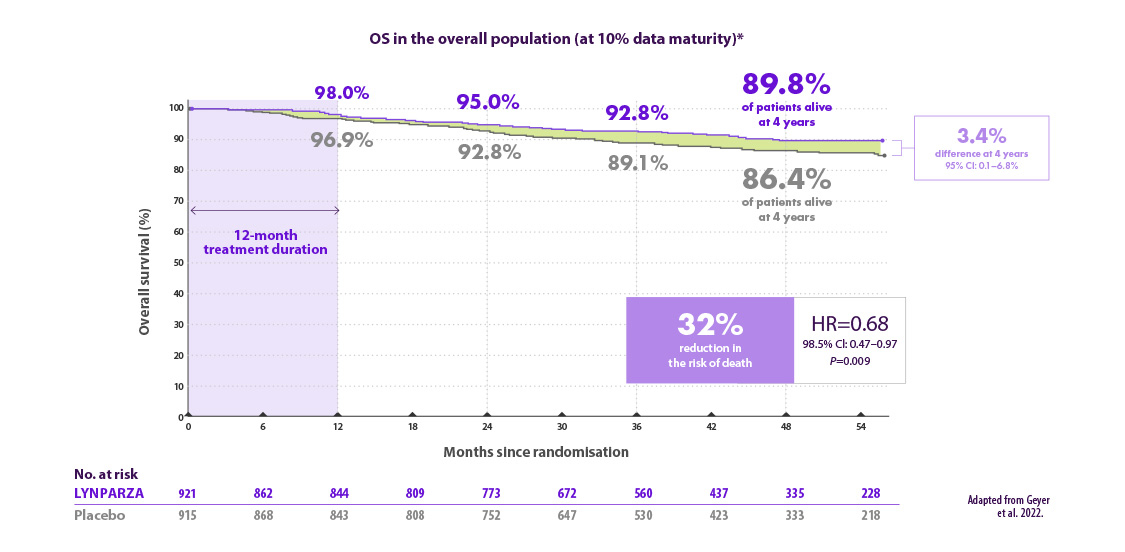
Lynparza® réduit de 32% le risque de décès par rapport au placebo7
Cancer du sein localement avancé ou métastatique (étude OlympiAD)
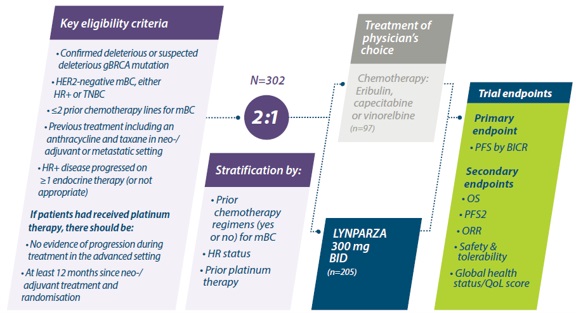
Conception de l’étude OlympiAD
L'étude OlympiAD était un essai de phase 3 randomisé, ouvert, dans lequel l'olaparib en monothérapie a été comparé à un traitement standard chez des patientes présentant une mutation germinale de BRCA et un récepteur du facteur de croissance épidermique humain de type 2 (HER2) négatif dans un cancer du sein métastatique et n'ayant pas reçu plus de deux chimiothérapies précédentes pour une maladie métastatique.8
Cancer du sein à un stade précoce (étude OlympiA)
Adapted from Robson M et al. 2017.
BICR=blinded independent central review; gBRCA=germline BRCA; HR=hormone receptor; HR+=hormone receptor-positive;
mBC=metastatic breast cancer; ORR=objective response rate; OS=overall survival; PFS=progression-free survival; PFS2=progression-free survival 2 (time to second progession); QoL=quality of life; TNBC=triple-negative breast cancer.
Résultats d’efficacité pour les patients atteints d’un cancer du sein métastatique HER2-négatif et présentant une mutation gBRCA1/2 dans l’étude OlympiAD
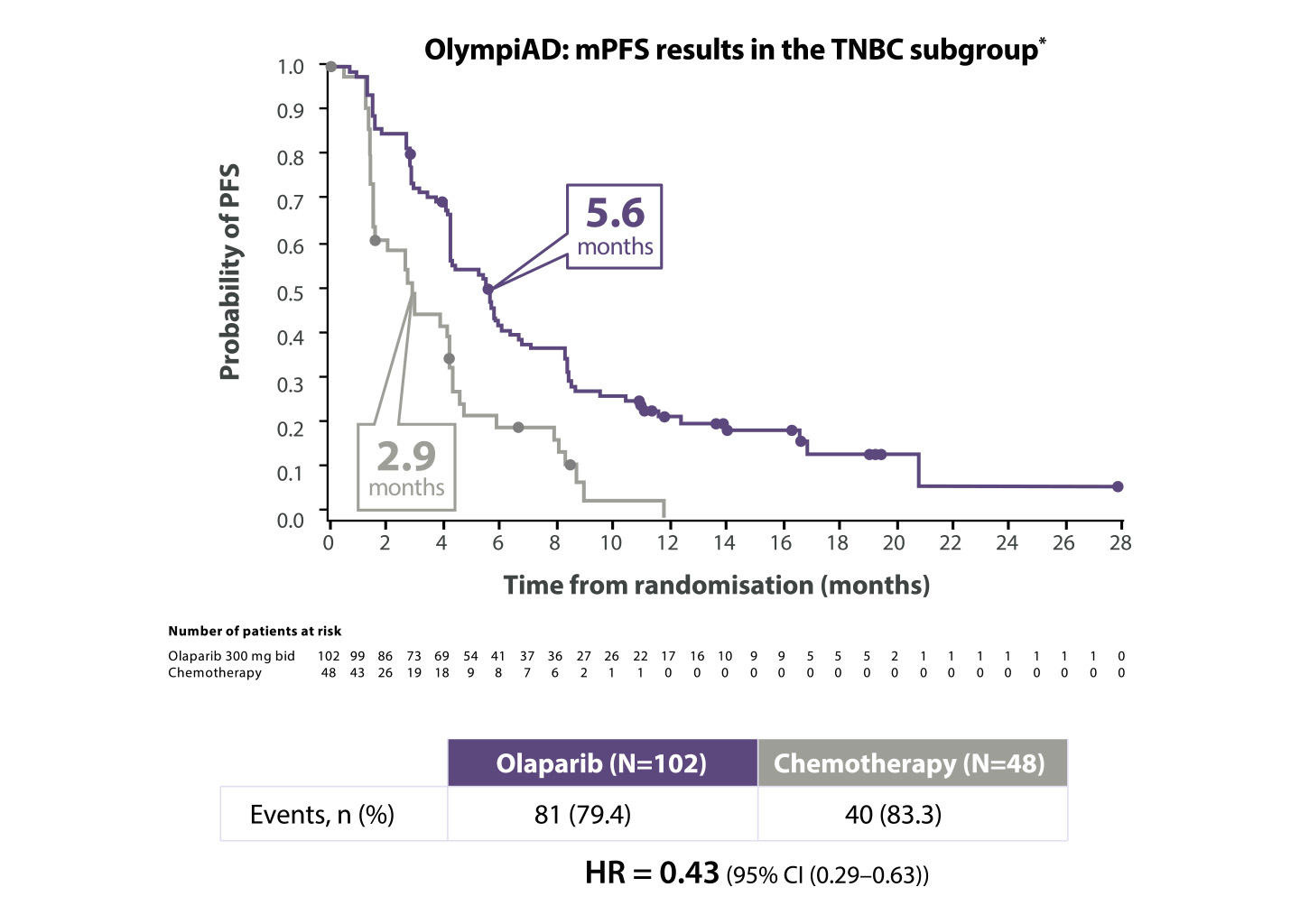
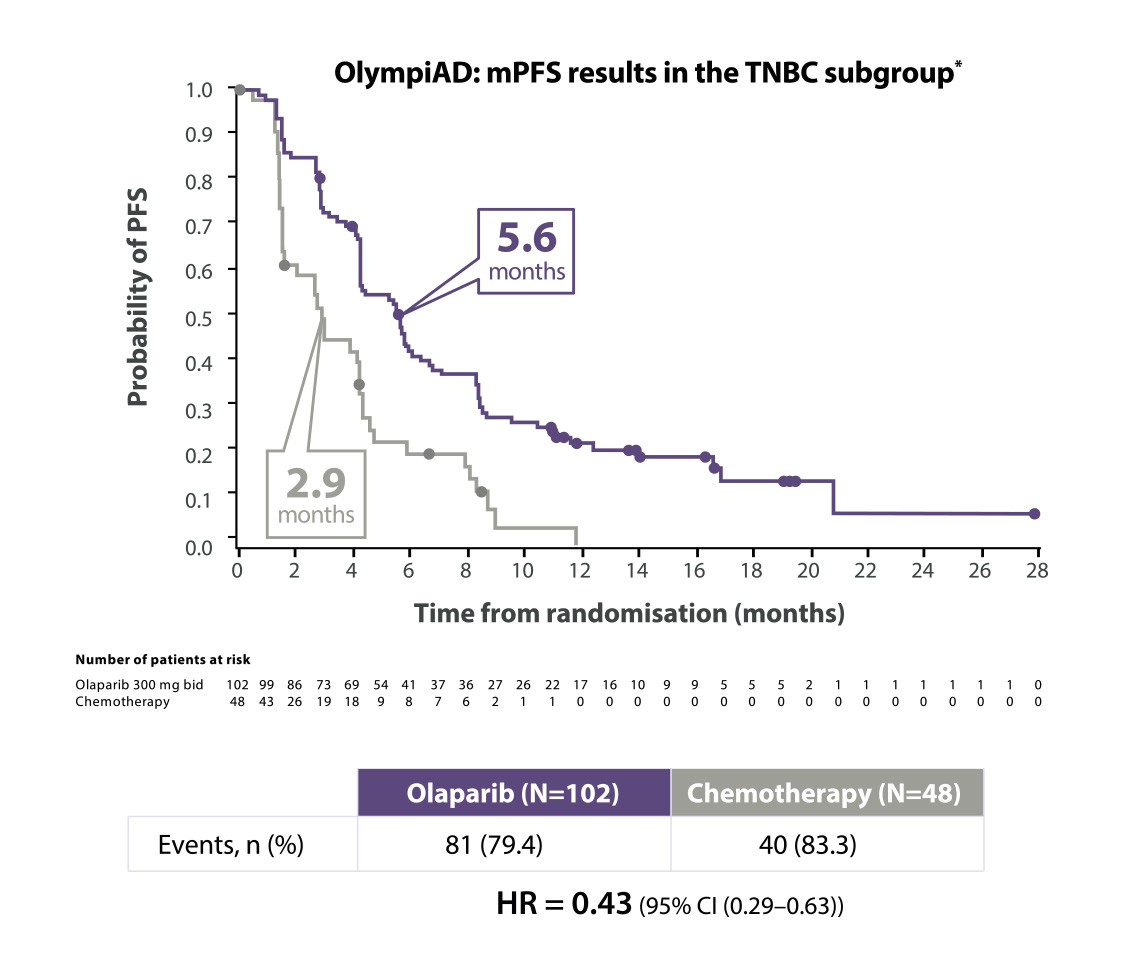
Lynparza® a doublé la SSP dans le sous-groupe TNBC9
Adapted from Senkus-Konefka et al. 2018
*The OlympiAD study was not powered to identify differences in treatment effect between subgroups, and any differences observed here are hypothesis-generating. Data cut-off: 9 December 2016
BID=twice daily; CI=confidence interval; HR=hazard ratio; (m)PFS=(median) progression-free survival; TNBC=triple negative breast cancer.
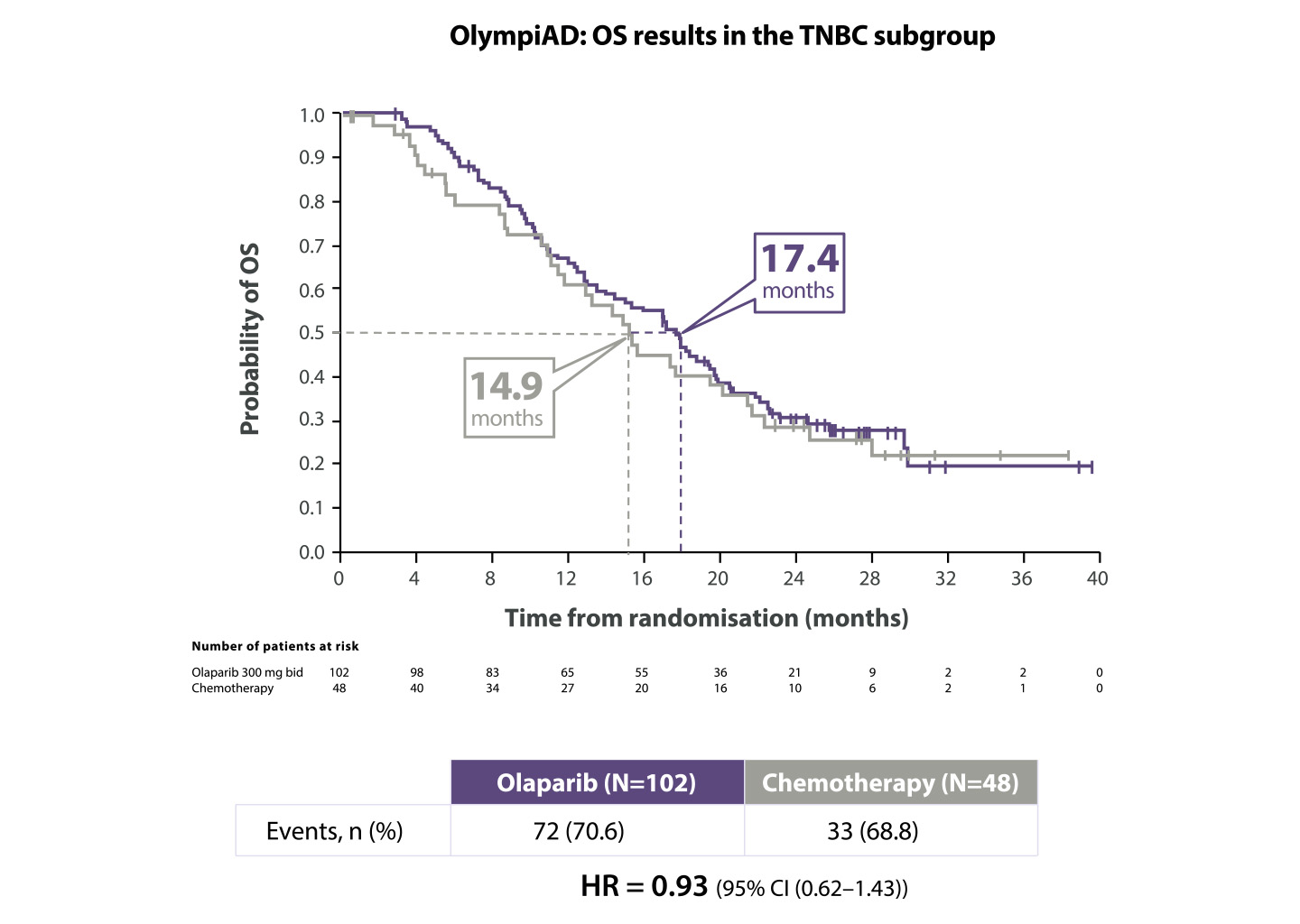
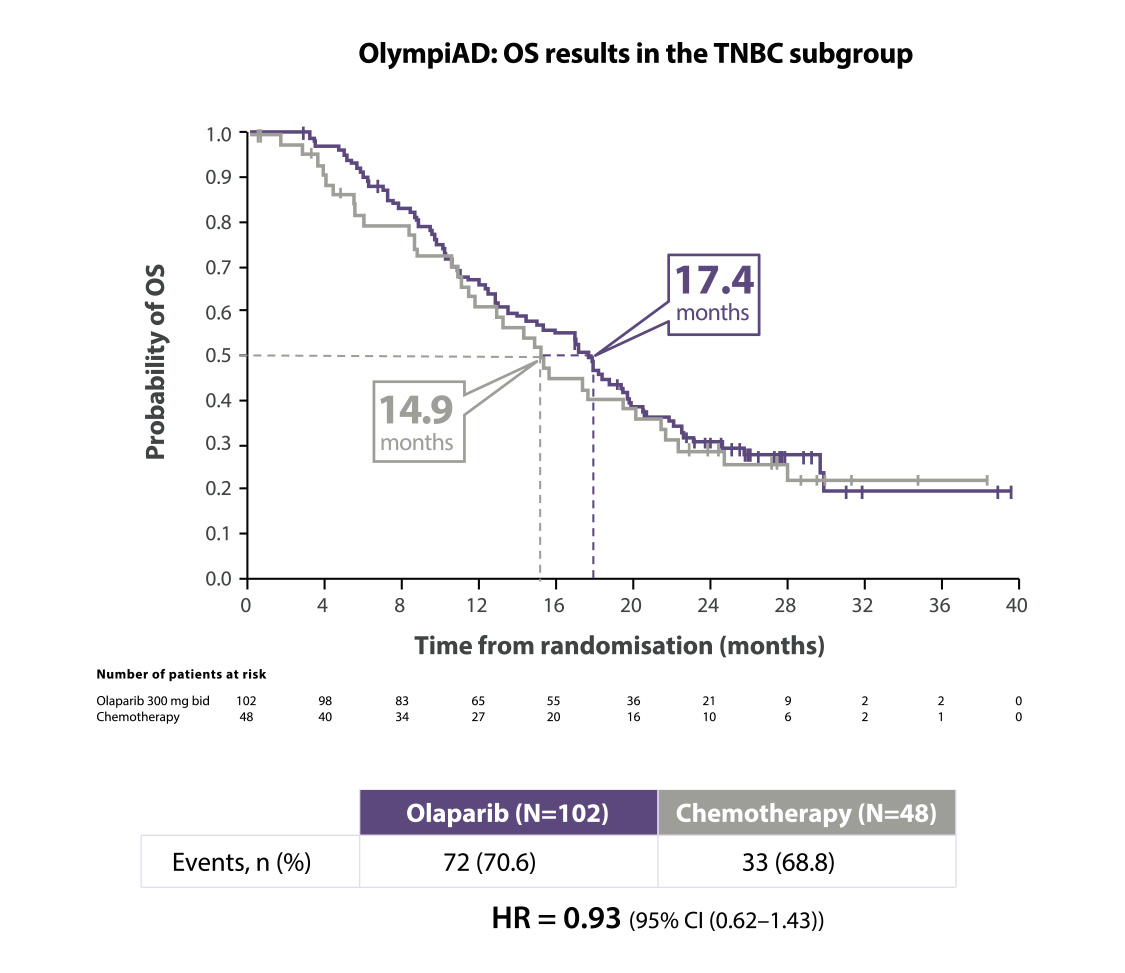
Lynparza® a amélioré l’OS dans le sous-groupe TNBC10
Adapted from Robson M et al. 2019.
* The OlympiAD study was not powered to identify differences in treatment effect between subgroups, and any differences observed here are hypothesis-generating. Data cut-off: 9 December 2016
BID=twice daily; CI=confidence interval; HR=hazard ratio; OS=overall survival; TNBC=triple negative breast cancer.
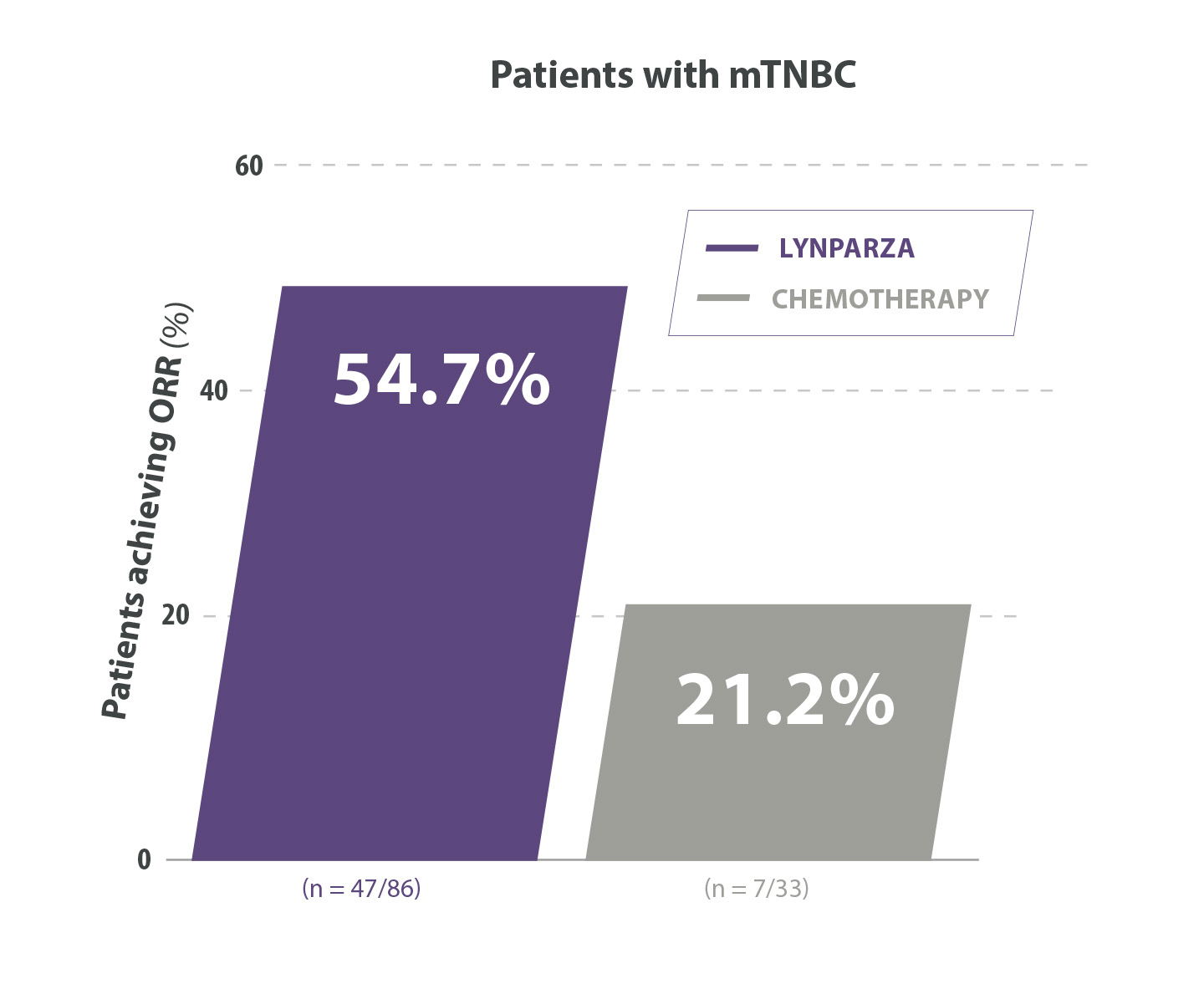
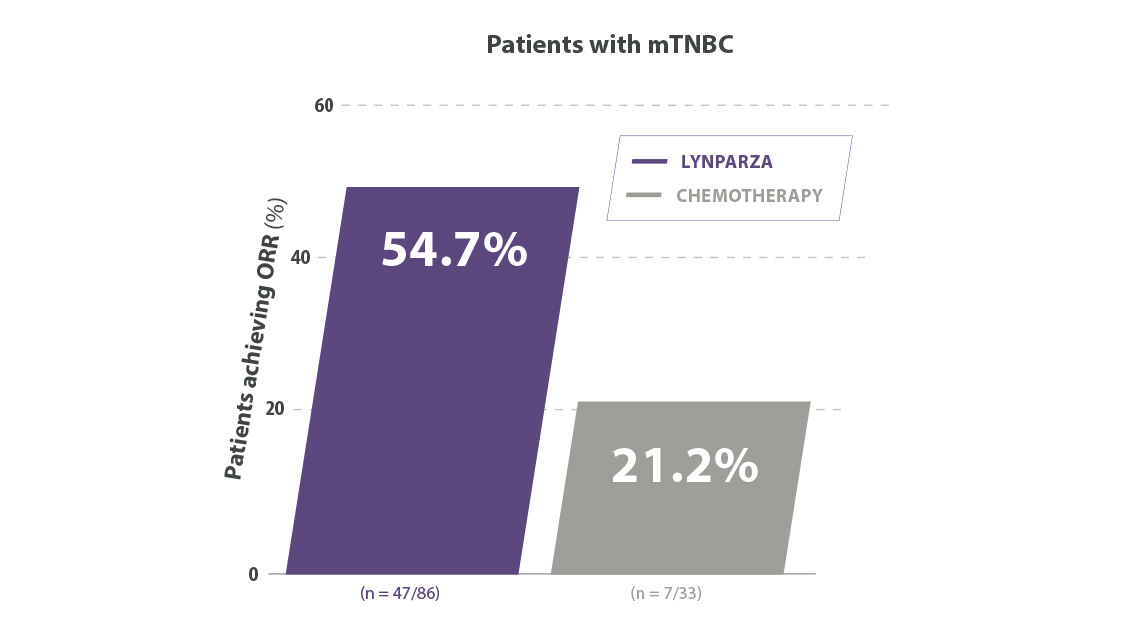
Lynparza® double l’ORR vs placebo dans le sous-groupe TNBC11
Adapted from Robson M et al. 2017. Supplementary appendix.
ORR=objective response rate ; TN=triple negative
Profil de sécurité
Cancer du sein précoce (étude OlympiA)
Effets indésirables rapportés chez ≥10% des patients de l'étude OlympiA*6
Adapted from Tutt ANJ et al. 2021.
*All listed are Grade 3 except for 10 Grade 4 events in the LYNPARZA group: Five events involving decreased neutrophil count, four involving anaemia, and one involving fatigue. AE=adverse event; AML=acute myeloid leukaemia; MDS=myelodysplastic syndrome
Environ 70 % des effets secondaires avec Lynparza® étaient de grade 1 ou 2.12
Il n'y a pas eu de différence significative dans la fréquence de syndrome myélo-dysplasique (SMD) ou de leucémie myéloïde aiguë (LMA) avec Lynparza® par rapport au placebo.6
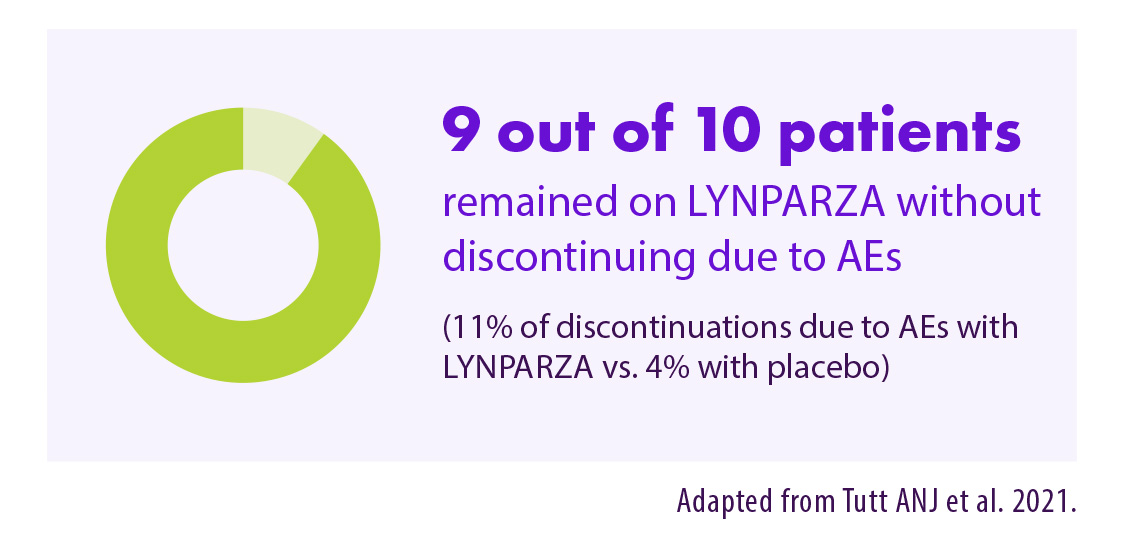
90 % des patients ont continué à prendre Lynparza® sans interruption en raison d'effets indésirables12
Adapted from Tutt ANJ et al. 2021. Supplementary appendix
Cancer du sein localement avancé ou métastatique (étude OlympiAD)
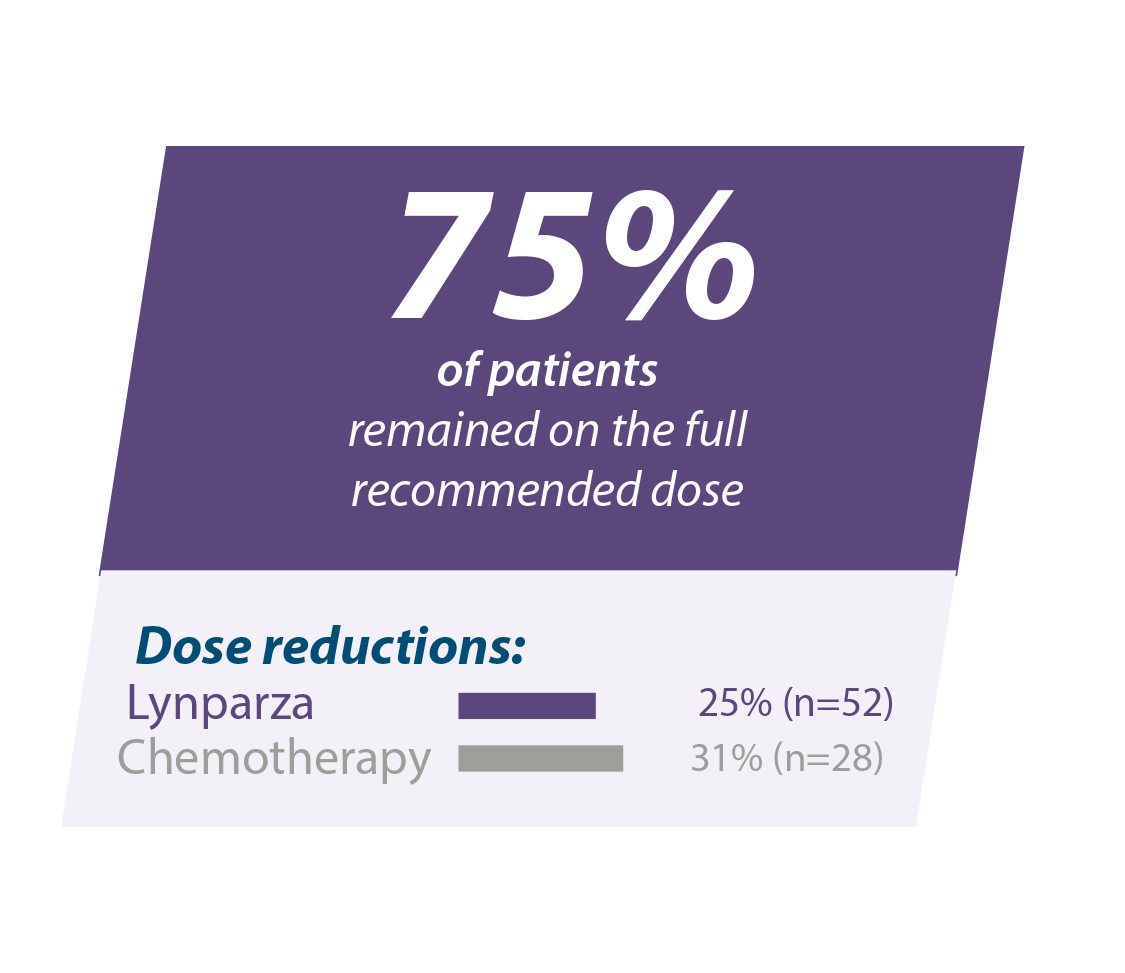
Les effets indésirables dans OlympiAD étaient pour la plupart d'une gravité légère à modérée, et gérables par des interruptions ou des réductions de dose.10
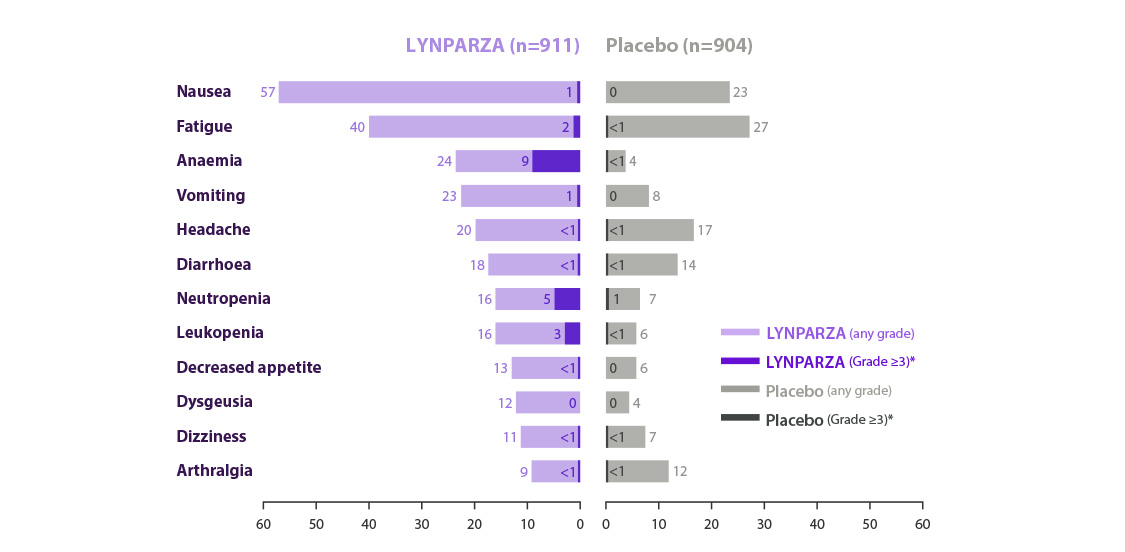
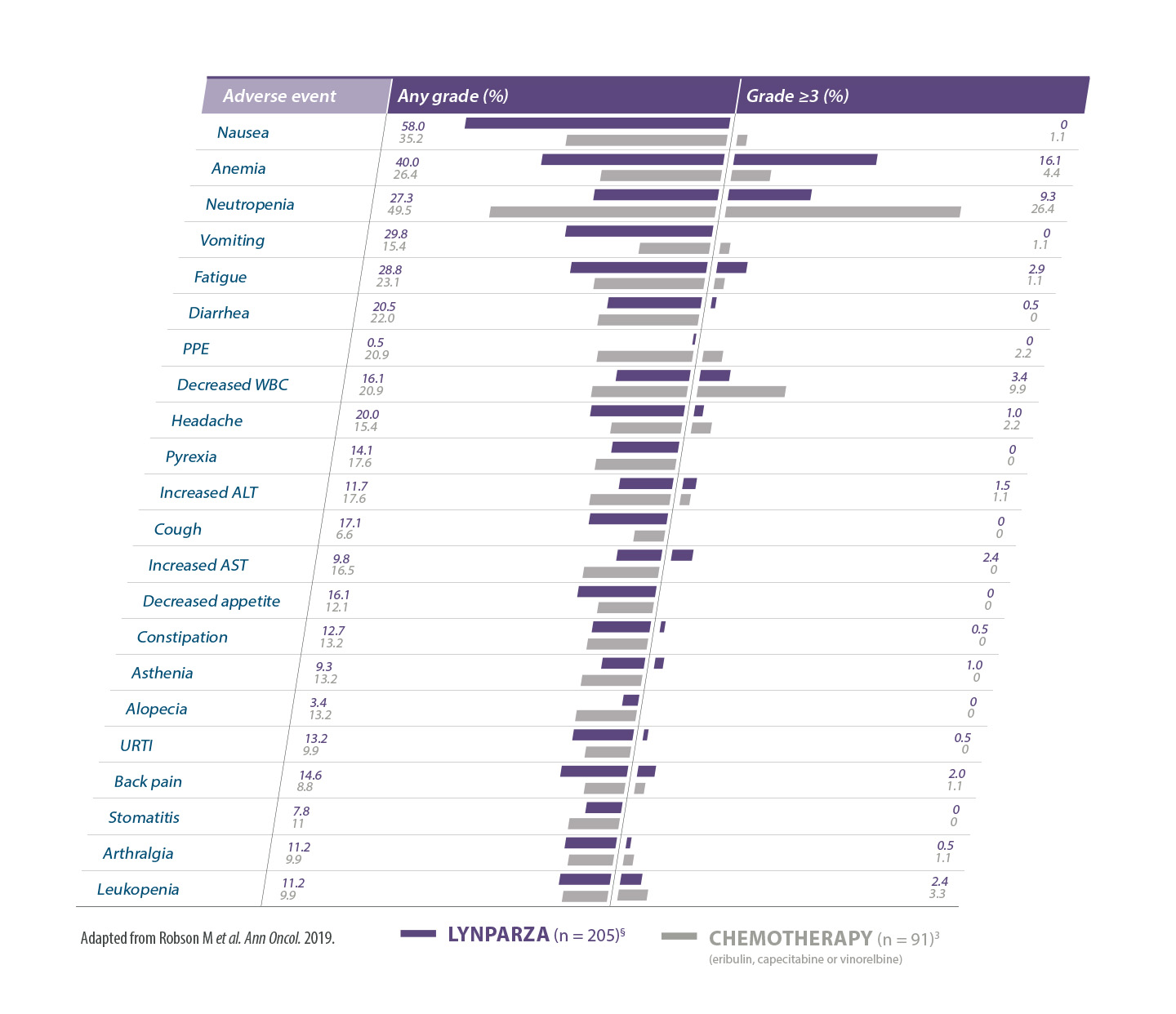
Effets indésirables rapportés chez ≥10% des patients de l'étude OlympiA*10
AEs of any cause; MedDRA-preferred terms are grouped for anemia (anemia, decreased Hb level, decreased hematocrit, decreased red blood cell count, and erythropenia) and neutropenia (febrile neutropenia, granulocytopenia, decreased granulocyte count, neutropenia, neutropenic sepsis, decreased neutrophil count, and neutropenic infection). ALT= alanine aminotransferase; AST= aspartate aminotransferase; PPE=palmar plantar erythrodysesthesia;.URTI=upper respiratory tract infection; WBC=white blood cells.
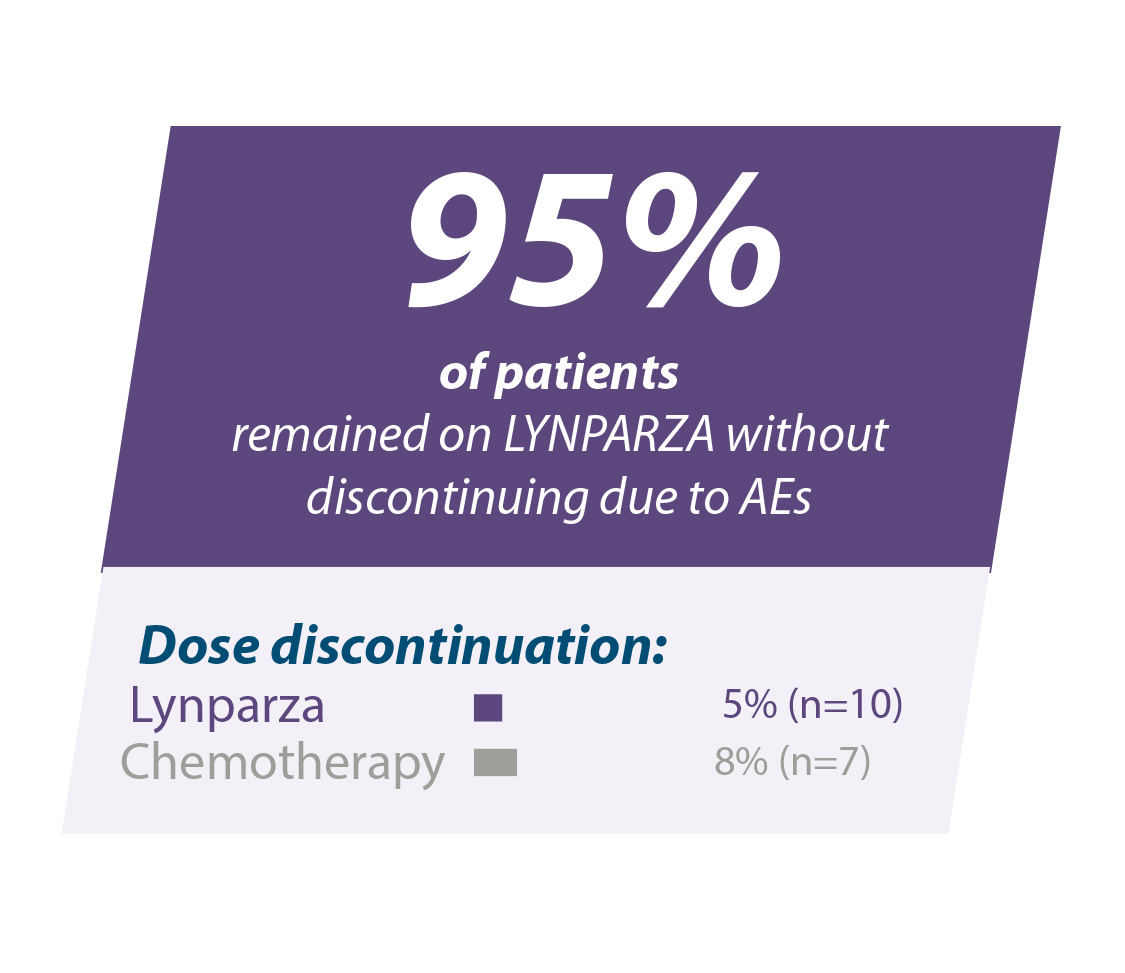
95 % des patients ont continué à prendre Lynparza® sans interruption en raison d'effets indésirables10
Recherche de mutations génétiques
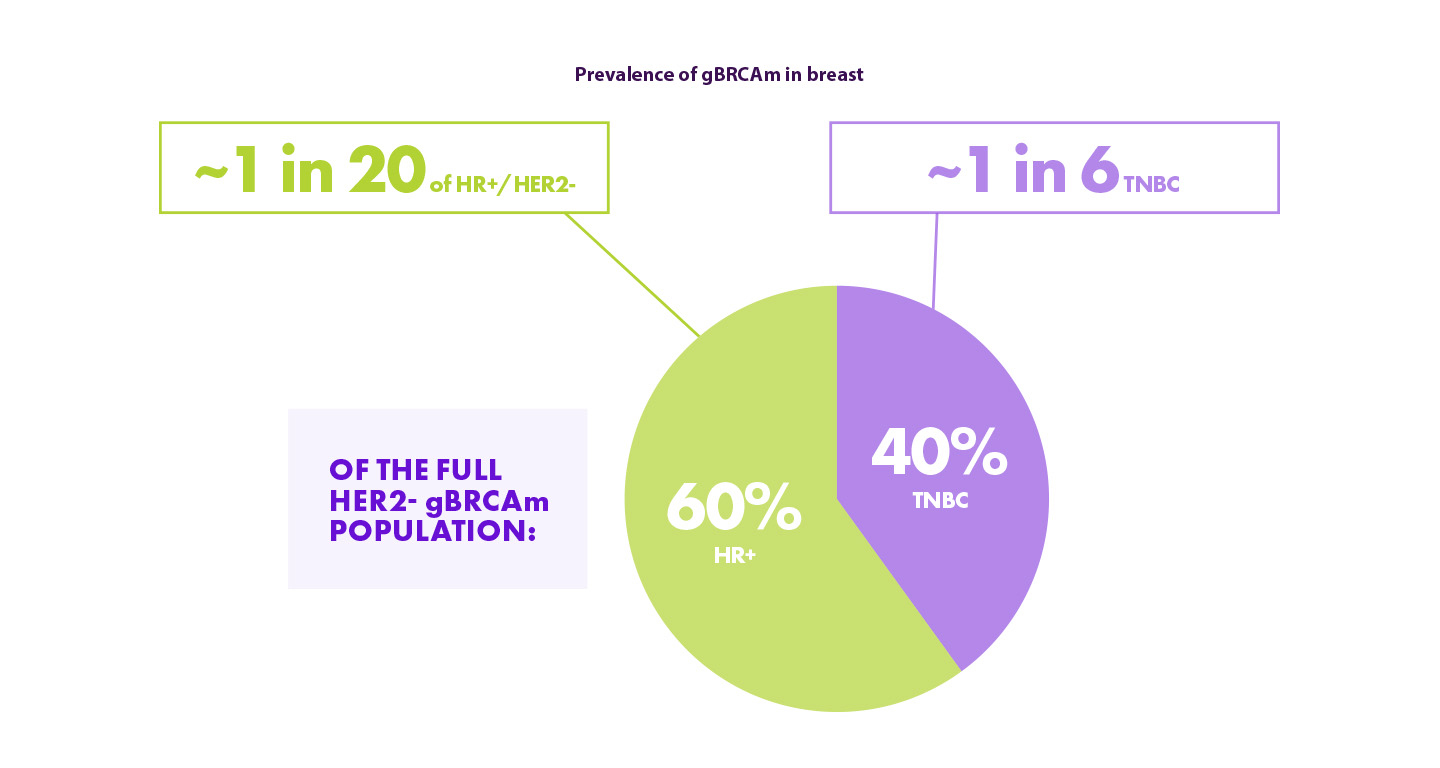
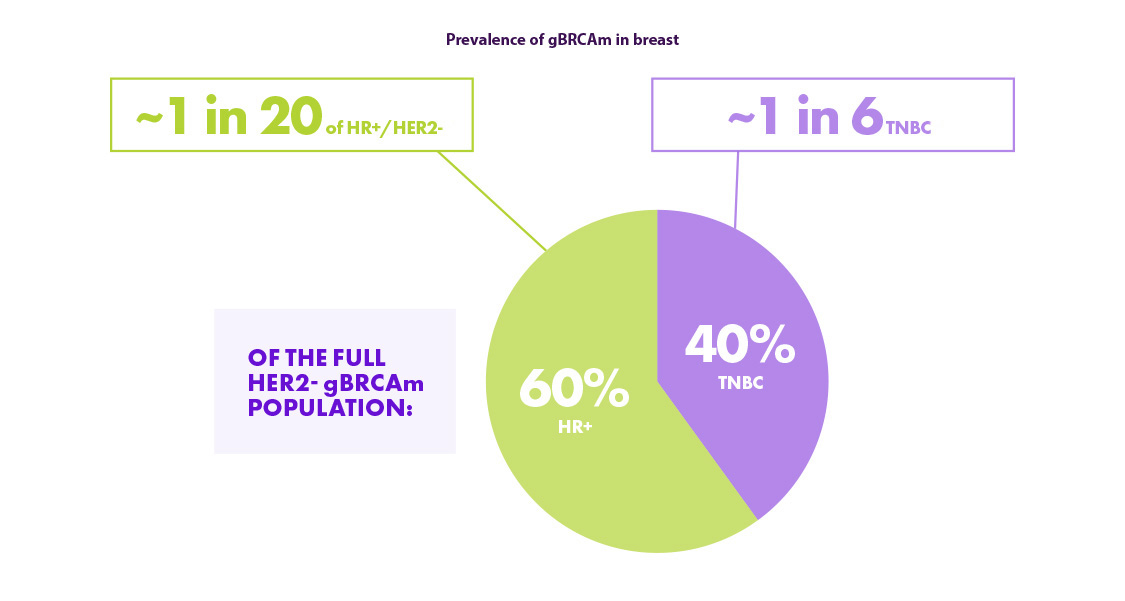
Bien que la prévalence de gBRCA dans le TNBC soit plus élevée que dans le HR+/HER2-, la majorité des patients HER2- gBRCAm sont des HR+ car le sous-groupe HR+/HER2- est plus grand.13,14
Il est donc important de ne pas négliger les patientes HR+ lors de la recherche de gBRCA.
gBRCAm = germline BRCA-mutated; HER2 = human epidermal growth factor receptor-2; HR+ = hormone receptor-positive; TNBC = triple-negative breast cancer.